„Az Alzheimer-kór nem egy titokzatos, kezelhetetlen agybetegség, hanem visszafordítható agyagcsere / toxikus rendszerbetegség, elég széles terápiás lehetőségekkel.” (Dale Bredesen)
Az Alzheimer-demencia (továbbiakban: AD) tüneteit nem ragozom, orvosi kezelése pedig egy szóban összefoglalható: kudarc. Inkább a betegség funkcionális koncepciójára fókuszálok, mely ígéretes kezelési lehetőségeket kínál az életmód átalakításával, céltudatos étkezéssel, célzott étrendkiegészítéssel.®
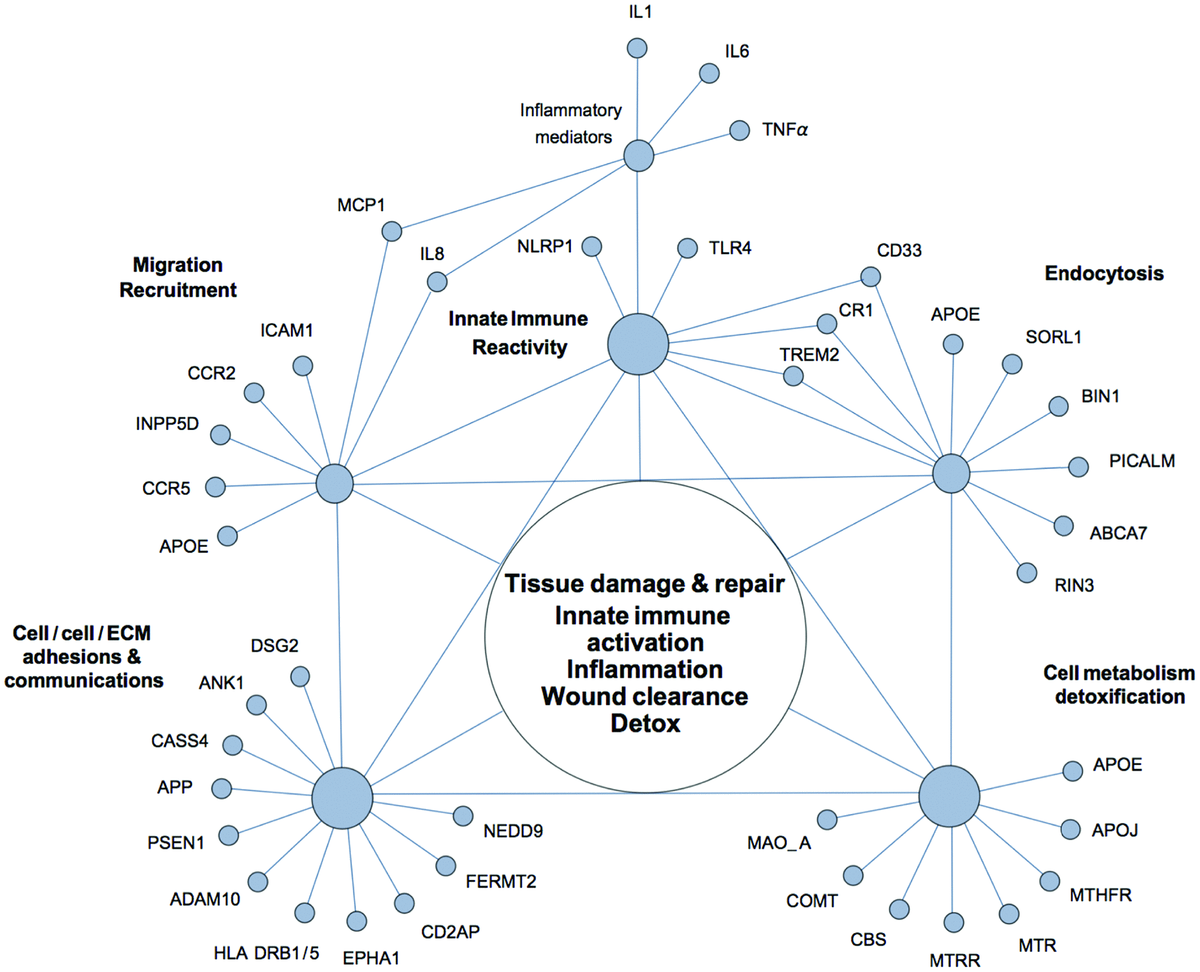 Kóros amiloid lerakódás? Elkerülhetetlen genetikai átok? Esetleg csak túl sokáig élünk, és szükségszerűen elbutulunk? Mindegyik, és egyik sem. A krónikus szellemi leépülésnek nincs egyetlen kizárólagos oka. A betegségnek számos fontos forrása van, melyek hátterében még több kiváltó ok található, ezek között pedig számtalan kölcsönhatás. Az idegrendszer leépülése a teljes szervezet betegsége, melyet csak akkor érthetünk, ha a rendszer egészét, és annak legfontosabb csomópontjait próbáljuk áttekinteni.
Kóros amiloid lerakódás? Elkerülhetetlen genetikai átok? Esetleg csak túl sokáig élünk, és szükségszerűen elbutulunk? Mindegyik, és egyik sem. A krónikus szellemi leépülésnek nincs egyetlen kizárólagos oka. A betegségnek számos fontos forrása van, melyek hátterében még több kiváltó ok található, ezek között pedig számtalan kölcsönhatás. Az idegrendszer leépülése a teljes szervezet betegsége, melyet csak akkor érthetünk, ha a rendszer egészét, és annak legfontosabb csomópontjait próbáljuk áttekinteni.
Bredesen és munkatársai 36 olyan tényezőt sorolnak,® melyek többé-kevésbé szövődhetnek, hatásuk hatványozódik, és közös végkifejletük: az ideg-hálózatok fokozatos leromlása. Legalább 36 méretes lyuk a háztetőn, melyből hiába foltozol néhányat: nem mentesít a beázástól. Az AD gyógyszeres kezelése azért kudarc, mert nincs olyan csodagyógyszer (monoterápia), mely képes lenne a (minimum) 36 problémás pontot lefedni.
Az Alzheimer-kór krónikus civilizációs betegségeink sorába illeszkedő rendszer-betegség, melynek következtében az agy lassú, krónikus gyulladásba merevedik.
Békeidőben az idegrendszer bővelkedik tápanyagokban, és energiaforrásban. Az idegsejtek szabadon működnek, hálózataik folyamatosan újraszerveződnek, új kapcsolatok épülnek (neuroplaszticitás). A békében használt agy: holtig tanul. Külső betolakodó (stressz, fertőzés) esetén erőteljes villámháborúval reagál (immunválasz, stresszreakció), majd lecsendesedik, és hamarosan visszatér nyugalmi, egyensúlyi állapotába.
Az Alzheimer-beteg agya azért kezd lepusztulni, mert (a később részletezett okok miatt) nem képes nyugalmi állapotába lecsendesedni. Az egyensúly (homeosztázis) visszaállítása elmarad, helyette a frontok megmerevednek, és krónikus gyulladás, tartós állóháború alakul.® A militarista beállítottságú genetikai örökség (lásd: apoE4) háborúzásra hajlamosít (és megmagyarázza, hogy miért éppen az agy lesz a krónikus betegség áldozata). Urbanizált környezetünkben számtalan (korábban ismeretlen) toxikus provokátor támadására kell reagálnia. Tartós háborús viszonyok között akadoznak a közszolgáltatások, ezért illegális szemétlerakók jelennek meg (lásd: béta-amioloid). A megmerevedett frontvonalak mögött az energiaéhes idegsejtek tápellátása akadozik (lásd: inzulin-rezisztencia). A határvidék (vér-agy gát) sérül, mert folyamatos (vegyi) támadások rombolják.® Az idegsejtek belső információs szerkezete, logisztikája sérül (mikrotubulusok), a lebombázott téglák halmokban hevernek. (hyperfoszforilált tau-protein). A háborúba merevedett idegsejt külkapcsolatai (szinaptikus hálózat) leépül. A kilátástalan állóháborúban sokan elpusztulnak (atrófia), mások visszahúzódnak, és alapvető túlélési üzemmódba kapcsolnak. A háborús agy gazdája felejt, és leépül. Az Alzheimer-kór nem más, mint lassú, romboló állóháború a koponyában.
Alzheimer esetén a krónikus gyulladást kísérő működési zavar leginkább az agyban mutatkozik, de a teljes rendszert kell gyógyítani! A kezelés célja a problémás kulcspontok feltérképezése, és a lehető legtöbb kritikus pont lefedése. Nézzük a legfontosabb szereplőket!
A szemétlerakódás: csak következmény!
Az Alzheimer-kór jellegzetessége: a halódó idegsejek környezetében (mikroszkóppal) látható jellegzetes szemétlerakatok, un. béta-amiloid kupacok, plakkok. Ezek a fehérje-kacatok az öregedéssel kisebb mértékben az egészséges idegsejtek körül is megtalálhatók, de a idegrendszer öntisztító mechanizmusai jórészt eltakarítják azokat.® AD esetén egyaránt gondot okozhat az amiloid fokozott képződése és az akadozó szemétszállítás.
A régi tudományos dogma szerint a szellemi leépülés okozója a béta-amiloid, mert akadályozza az idegsejtek működését. Újabban úgy vélik, hogy az amiloid-képződés csak kísérője számos kórfolyamatnak. Az amiloid részt vesz például az idegrendszerbe került kórokozók elszigetelésében.® A kártékony behatások aktíválják az agy immunrendszerét (mikroglia), ami fokozott amiloid-termelést provokál. A béta-amiloid felszaporodása tehát inkább a károsodott idegrendszer védekezését mutatja. Ennek ismeretében érthető az amiloid-lerakódást csökkentő gyógyszerek kudarca, hiszen csak a következményt kezelik.
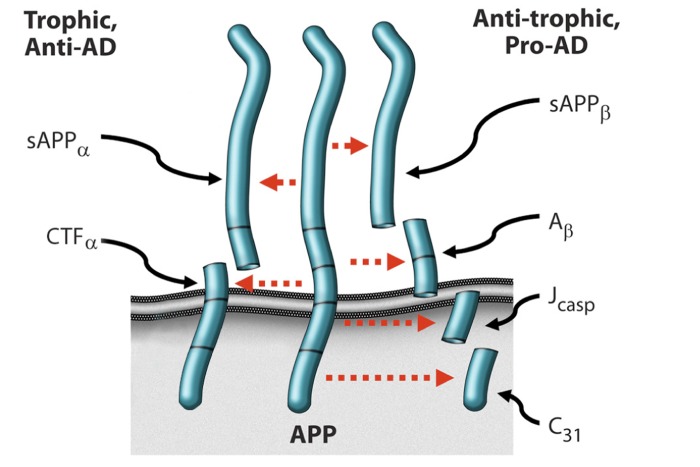
A béta-amiloid forrása az APP (amiloid precursor protein). Az idegsejtek felszínéről kilógó fehérjét számos enzim darabolhatja annak megfelelően, hogy milyen környezetben működnek.® Békeidőben (az ábra bal oldalán) az APP két részre hasad, melynek terméke (sAPPα) az idegsejtek szaporodását, növekedését, egészséges működését támogatja. Háborús viszonyok között más hasítóenzimek aktívak, ennek nyomán az APP négy részre hasad, melyek egyike az összecsapzódásra hajlamos béta-amiloid. Egészséges agyban is termelődik béte-amiloid, hiszen tudjuk, hogy szerepe van pl. a kórokozók megfékezésében. AD esetén azonban meghatározóvá válik az APP háborús típusú hasítása, így az arány eltolódik az összecsapzódásra hajlamos változat javára. A probléma tehát nem maga az amiloid, hanem a tartós hadiállapot, mely rendellenes mederbe tereli egy fontos molekula életútját.
Az AD legerősebb ismert genetikai meghatározója az apolipoprotein-E 4-es változata. Aki egyik szülőtől örökli (2-es, 3-as helyett) a 4-es típust, abban (az átlagos 9% helyett) 30% eséllyel kialakul élete folyamán az elbutulás. A népesség 2%-a mindkét szülőtől ilyet kap, esetükben több, mint 50% a betegség kialakulásának esélye. Ez 12-szeres rizikót jelent! Mit tud ez a fehérje?
 Az apo-E az idegrendszer zsíranyagcseréjében alapvető hordozó-anyahajó. Szállító szerepe fontos lehet, hiszen az idegrendszer (víz nélkül) 60-70% zsírból áll. Ezen túlmenően az apo-E számtalan gén működését módosítja, és számos anyagcsere-folyamatban részes. (Béta-amiloid kezdeti felszaporodása, tau-protein módosítása, agyi erek integritásának fenntartása, szinaptikus kapcsolatok ápolása, inzulin-hatás támogatása.)®
Az apo-E az idegrendszer zsíranyagcseréjében alapvető hordozó-anyahajó. Szállító szerepe fontos lehet, hiszen az idegrendszer (víz nélkül) 60-70% zsírból áll. Ezen túlmenően az apo-E számtalan gén működését módosítja, és számos anyagcsere-folyamatban részes. (Béta-amiloid kezdeti felszaporodása, tau-protein módosítása, agyi erek integritásának fenntartása, szinaptikus kapcsolatok ápolása, inzulin-hatás támogatása.)®
Ami pedig talán a legfontosabb: az apoE meghatározó szerepet játszik az idegrendszer veleszületett immunrendszerének aktíválásában.® Az apo-E4 altípus különlegessége pedig az, hogy határozottan sértődékeny.® A legkisebb fenyegetést is támadásként értelmezi, és aktivizálja, védekezésre hangolja az immunrendszert. Az apo-E4 a család szélsőjobbos, militarista tagja. Ez a harcos attitűd évmilliókon keresztül hasznos volt a vadász-gyűjtögető életmód óhatatlan sérüléseinek túléléséhez. Egy rövid, harcos karrier során az apoE4 hatékonyan segített, ezért 7 millió évig ez volt az eredeti génváltozat.
Aztán megváltoztak életkörülményeink: ma már 100 évig szeretnénk békességben élni. Pusztán néhány száz generációval ezelőtt mutálódott az ősi apoE4-ből E3, majd E2 változat, melyek hosszas békeidőben előnyösebbnek bizonyultak. Az egykori vad forma villámgyorsan kiszelektálódott, és ma mindössze az emberek 2%-a őrzi az E4 génpárt. Bennük a hosszabb életút során visszájára fordul az egykori csodafegyver: az évtizedeken keresztül húzódó enyhe gyulladás lassan felőrölheti az agyat.
A militarista apoE4 tehát alapjaiban meghatározza az idegrendszer alap-beállítását, gyulladás-készségét. Érdemes itt megjegyezni, hogy az AD második legfontosabb genetikai rizikója (a TREM2 gén egyik változata) szintén az agy immunsejtjeinek (mikroglia) aktiválásán dolgozik.
A gyulladásos agy.
A gyulladásos típusú Alzheimer-beteget enyhe, de hosszasan elhúzódó immun-válasz pusztítja, és a fentiekből érthető, hogy e forma igen gyakran apoE4 genotípussal társul. A leépülést kísérő jellegzetes laborleletek (hsCRP↑, TNF-α↑, albumin/globulin arány↑) krónikus gyulladásról árulkodnak. Krónikus gyulladást provokálhatnak az ócska növényi olajok, melyek kórosan fokozzák az omega-6 zsírsavak arányát.® Az elhúzódó gyulladás kiváltóját nem mindig tudják igazolni, máskor egyártelmű krónikus fertőzések is kimutathatók. Gyakori góc az elhanyagolt fogazat (foggyökér granulóma), melynek jellegzetes kórokozóit meglepően gyakran találják elhunyt Alzheimer-betegek agyában.® Krónikus fertőzést okozhat a Borrelia (Lyme-kór), és további kullancs által terjesztett kórokozók (Bartonella, Babesia). Vírusok sora is krónikus fertőzést okozhat az agyban (HSV, EBV, CMV, HIV).
Az agy diabétesze?
Az Alzheimer-kór szorosan kapcsolódik a teljes anyagcsere, energiatermelés és elosztás rendszerhibáihoz. Ez nem meglepő, ha az agy extrém energia-éhségére gondolunk: a testtömeg pusztán 2%-át kitevő szerv (nyugalomban) a teljes tüzelőfelhasználás 20%-áért felelős. A tüzelő-kínálatból (glükóz, és zsírsavak) agyunk szinte kizárólag csak a glükózt képes égetni. Koplalás idején testünk zsírégetésre vált, a máj pedig ketonokat termel, melyek az agy számára is alkalmas kiegészítő tápanyagok.
Az Alzheimer-kórt olyan gyakran kíséri inzulin-rezisztencia (IR), hogy egyes szerzők® egyenesen 3. típusú diabéteszként említik.® Az inzulin-emelkedés ilyenkor gátolja a ketontermelést, a leromló inzulinhatás pedig akadályozza a glükóz-hozzáférést. Az IR ilyen módon mindkét lehetséges üzemanyagától megfosztja az energiaéhes agyat! AD esetén a cukor-felhasználás zavara korai jel: évtizedekkel korábban kimutatható®, mint az amiloid megjelenése,® és a demencia kialakulása.® A fentebb említett apo-E4 számos hatása mellett az inzulin-receptort is akadályozza.® Apo-E4 hordozókban különösen hamar, akár a 20-as életévektől megfigyelhetők csökkent cukorfelvételű agyterületek – mégpedig ugyanott, ahol később a demencia pusztít.®
Az IR az előrehaladott AD másik mikroszkópos jellegzetességében (kóros tau-protein) is szerepet játszik. Az idegsejtekben összecsapzódott un. neurofibrilláris gubancok alkotója: foszforilált (foszfát-csoportokkal teletűzdelt) tau-protein. E számos funkciót betöltő fehérjék részt vesznek az idegsejt belső szerkezeti vázának (mikrotubulus-hálózat) felépítésében. A foszforilációért felelős enzim nem más, mint a glikogén-szintáz-kináz (GSK3béta). Normál esetben ennek működését az inzulin fékezi. Inzulin-rezisztancia esetén ez a fék nem működik, ezért az elszabadult GSK3béta több foszfort pakol a tau-fehérjére, mely összegubancolódik, összecsapzódik.® A korábbiakban felszaporodott béta-amiloid ráadásul közvetlenül is serkenti a kináz enzimet, ezzel maga is hozzájárul a kóros tau-protein felszaporodásához.®
Az inzulin-rezisztencia tehát mindkét jellegzetes AD-tünet (béta-amiloid, és patológiás tau) kialakulásában szerepet játszik. Az IR mégsem tekinthető a betegség közvetlen (és még kevésbé egyedüli) okának. Nyugati országokban az IR nagyon gyakori, de nem egyetlen forrása az agy leépülésének.
Az inzulin-rezisztencia rontja az idegsejtek tápanyag-ellátását, ugyanakkor kevésbé érvényesül az inzulin építő (anabolikus) hatása, és mindkét tényező a pusztulás felé hajtja az idegsejteket. A problémát jelzik a laborban a metabolikus szindróma markerei (triglicerid↑, HDL↓). Ilyenkor speciális mérésekkel (HOMA-IR, inzulin méréssel kiegészített OGTT) érdemes tisztázni az inzulin-rezisztencia súlyosságát. (Érdekességként: egyik Alzheimer-gyógyszerünk (Galsya) nem mellékesen: hatásos gyulladáscsökkentő, és javítja az inzulin-rezisztenciát.® Lehet, hogy éppen ez a fő oka hatékonyságának...)
A kiéhezett agy.
A szellemi leépülést esetenként nem a gyulladás, vagy IR uralja, hanem az agyat éltető, tápláló (trofikus) faktorok hiánya. Az apoE4 pozitivitás ritkább e típusban, helyette inkább általános hormonzavar látható. A laborban jellemzőek a mellékvese-kifáradás jelei (kortizol↓, DHEA↓, pregnenolon↓), csökkent lehet a pajzsmirigy-működés (TSH↑, T3↓, T4↓ reverz T3↑), és általában csökkent szexhormonok (tesztoszteron, ösztrogén, progeszteron) láthatók. Gyakran csökkent a D-vitamin, folsav, B6, B12®, ugyanakkor emelkedett lehet a homocisztein®.
A mérgezett agy.
Méltatlanul kevés figyelmet kapnak az Alzheimer-kórt kísérő krónikus mérgezések. A toxikus károsodást okozhatják nehézfémek, gombatoxinok, kemikáliák. Hatásukra előfordul, hogy a mentális hanyatlást a kérgi károsodás dominálja, ezért memóriazavar helyett más vezető tünetek jelentkeznek: karakterváltozás, és a szótalálás, számolás, olvasás, írás nehézségei. Esetleg más betegség képében (frontotemporális demencia, depresszió) jelentkezhet az agy krónikus mérgezése.
A réz vízvezeték krónikus réz-túlterhelést okozhat, melynek rendszeres kísérője a cink-hiány, a cink/réz arány csökkenése. (A két fém gátolja egymás felszívódását.) Hasonló cink-hiány okozhat a savkötő gyógyszerek (protonpumpa-gátlók) tartós szedése.® Tengerparti régiókban probléma lehet a rendszeres halfogyasztással érkező higany-terhelés. Tájunkon inkább az évtizedeken keresztül használt amalgám-fogtömés merül fel a krónikus higany-mérgezés hátterében.® Az ólmozott benzin kivonásáig az urbanizált régiók legnagyobb terhelését a kipufogógázok ólom-szennyezése adta. Az alumínium kóroki szerepe ma sem tisztázott, de rendre felmerül a krónikus fém-mérgezések sorában.® A fém-mérgezésekről tudni érdemes, hogy a kötött állapotban lapuló nehézfémeket a vérből végzett laborvizsgálat nem feltétlenül képes kimutatni. Igazolásához speciális (kelátképző) segédanyagok, és a gyűjtött vizelet vizsgálata lehet szükséges.
Az agyat pusztító krónikus mérgezést okozhatnak a gombatoxinok is. (Aflatoxin, penészgombák.) Ennek jellegzetes labormarkere lehet a triglicerid/összkoleszterin arány csökkenése, vagy a C4-a komplementer emelkedése.
A korai diagnózis: agyat ment!
Irásom az időskori Alzheimer-kórt taglalja, de tudni kell, hogy a betegség kezdete, mentális teljesítmény csökkenése célzott vizsgálatokkal már évtizedekkel korábban kimutatható. Ez a bevezető állapot (enyhe kognitív károsodás) sokkal kedvezőbb terápiás lehetőségekkel kecsegtet, ezért akár szűrő jelleggel is keresni érdemes. Családi halmozódás esetén már fiatal korban indokolt az apoE genetikai vizsgálata. Az érintett agyterületek töpörödését később objektíven mutatja az MR-volumetria. Az agykérgi dominanciát mutató toxikus károsodást korán igazolhatja egy speciális koponya-MR technológia (T2 súlyozott FLAIR szekvencia). Minden AD esetén tisztázni kell az inzulin-rezisztenciát (triglicerid, HDL-koleszterin, HOMA-IR, éhomi inzulin, OGTT)
A gyulladásos laborok (hsCRP, TNF-α, albumin/globulin) mellett a teljes hormonális státusz felmérése indokolt. Célirányosan keresni érdemes a krónikus fertőzéseket. Tisztázandó a vitaminok (D, B6, folsav, B12), ásványok (cink, réz, magnézium, vas) vérszintje. Gyanú esetén toxikus nehézfémek után kell kutatni.
Az Alzheimer-kórt okozó rendszer-hiba legfontosabb összetevőinek feltérképezése komoly kutatómunka, de nem megspórolható. Csakis erre alapozható érdemi terápia.
Terápia.
Az egészséges agyi metabolizmus négy pillére: az étkezés, koplalás, testgyakorlás, és alvás.
Az inzulin-érzékenység helyreállítása az első legfontosabb teendő (lásd ott is). A diéta célja a mérsékelt (intermittáló) ketózis. Ennek eszköze a rostokban gazdag, zöld növényekre alapozott low-carb étrend egészséges zsírokkal, és mértékletes fehérjefogyasztással. A finomított szénhidrátok (cukor, keményítő), gabonafélék® (lásd: cöliákia) elhagyása mellett fontos kiiktatni a említett kártékony növényi olajokat, és a lehető legtöbb feldolgozott, tartósított élelmisz@rt. Az ételszemét gyulladáskeltő, és IR-t okoz. Valódi élelem nélkül nincs gyógyulás.
A táplálkozási ketózisból származó ketontestek alternatív tüzelőanyagot kínálnak a kiéhezett agy számára.® A vizsgálatok szerint az étrendkiegészítőként alkalmazott keton-pótlás is előnyös.® A kívülről bevitt (exo)keton jótékony hatása dózis-függő®, ami arra utal, hogy a folyamatos, magasabb keton-szintet biztosítani képes ketogén diéta még előnyösebb, és talán legjobb a kettő kombinálása. A ketózis mélyítésére MCT-pótlás is használható. (ApoE4 pozitivitás esetén telített zsírok helyett inkább olívaolaj tanácsolható.)
Az étrend kiegészítésére célirányos vitamin-, és ásványpótlás indokolt (B-komplex, C, D, E, K2, Cink, Mg, szelén). Segíthet a melatonin, kolin, és omega-3 pótlás, berberin, fahéj.
A jól felépített étrend hetek alatt helyreállítja az inzulin-érzékenységet. Ezt követően mértékletes koplalás, időben korlátozott étkezés egészíti ki a terápiát. Bredesen munkacsoportja 12 órás étkezési ablakot javasol, és fekvés előtt 3 órával már tiltja az étkezést. ApoE4 pozitivitás esetén szigorúbb korlátozást, napi 8 órás érkezési időablakot javasolnak. (Később a napi 1 étkezés is megpróbálható.) A low-carb étrend mellett ez jelentősen mélyíti a ketózist, különösen a terápia következő elemével, a rendszeres testgyakorlással együtt. A mozgás látványosan növeli az agyi növekedési faktor (BDNF) termelődését. 6 hónap testgyakorlástól az idősödő emberek agya határozott növekedést mutat, különösen a memóriáért felelős területeken.®
A komplex terápiának része kell legyen az aktív stressz-kezelés. A krónikus pszichoszociális stressz ismert forrásait (gyermekkori trauma, egzisztenciális kitettség) egyéni és csoportos pszichoterápia, támogató csoport segíthet megemészteni. A tüneti stressz-kezelés eszköztára kimeríthetetlen. (Természetjárás, csapatsportok, jóga, meditáció, mindfulness, autogén tréning, biofeedback, neurofeedback.)
A krónikus stressz gyakori forrása az alváshiány. Az Alzheimer kezelésének is sarkalatos pontja a megfelelő alvás-higiéne. Elengedhetetlen az alvási apnoe kizárása, esetleges kezelése (CPAP-készülék). Fontos a Nap járásához illeszkedő alvási ritmus. Napnyugta után kerülendő a TV, monitor, és mindenféle kék fényforrás (LED). A hálószoba ne legyen 19 foknál melegebb. Az elalvás segítésére melatonin-pótlás is mérlegelendő. Az előző pontok (étkezés, koplalás, testgyakorlás) sikerének fontos jele az alvás minőségének javulása. Ennek ellenőrzését segítheti egy okos óra, vagy gyűrű.
Emlékeztetőül: az Alzheimer-kezelés sikeréhez nélkülözhetetlen a krónikus mérgezések, fertőzés-források feltérképezése, célzott kezelése (szájhigiéné, penészmentesítés, Lyme-kezelés, stb.). Az esetleges nehézfém-mérgezés felszámolásához fogtömés-csere, kelát-terápia, víztisztító felszerelése lehet szükséges.
A komplex terápiás program gyakorlatba ültetése súlyosan leépült betegnél szinte lehetetlen. Ez aláhúzza a korai diagnózis fontosságát! Az enyhe kognitív károsodás felismerése: lehetőség a gyógyulásra!
Összefoglalás.
Az ismertető erősen technikai jellegűre sikeredett (még így is hiányos), de reményem szerint rámutat, hogy a szellemi hanyatlásnak számtalan forrása lehet, és kezelése sem állhat 1-2 tabletta szedéséből. A rendszer-hiba főbb forrásainak feltérképezésével azonban számos terápiás lehetőség nyílik a leépülés megállítására.
A részleteket illetően kollégák számára ajánlom a referenciák (és azok referenciáinak) böngészését. Érintettek, és hozzátartozóik számára pedig erősen javaslom Dr. Dale E. Bredesen nagyközönség számára írott könyvét: Az Alzheimer-kór vége. Angol nyelven már ennek folytatása is megjelent az időközben kibővített, átdolgozott terápiás programmal.
- Avila J et al: Tau Phosphorylation by GSK3 in Different Conditions. Int J Alzheimers Dis. 2012; 2012: 578373.
- Beydoun MA et al: Vitamin D, Folate, and Cobalamin Serum Concentrations Are Related to Brain Volume and White Matter Integrity in Urban Adults. Front Aging Neurosci
. 2020 May 25;12:140. - Bredesen DE: Reversal of Cognitive Decline: A Novel Therapeutic Program. Aging 6, 9 (2014): 707–17.
- Bredesen DE et al: Reversal of cognitive decline in Alzheimer’s disease. Aging 8: 1250–1258. (2016).
- Brewer, G. J. Copper excess, zinc deficiency, and cognition loss in Alzheimer’s disease. Biofactors 38: 107–113. (2012).
- Colcombe SJ et al: Aerobic Exercise Training Increases Brain Volume in Aging Humans. The Journals of Gerontology: Series A, Volume 61, Issue 11, November 2006, Pages 1166–1170.
- Consoli-Colombo FM et al: Galantamine alleviates inflammation and insulin resistance in patients with metabolic syndrome in a randomized trial. JCI Insight. 2017 Jul 20;2(14):e93340.
- Cunnane SC et al: Brain Fuel Metabolism, Aging, and Alzheimer’s Disease. Nutrition 27, no. 1, 3–20, January 2011.
- Cunnane SC et al: Can Ketones Help Rescue Brain Fuel Supply in Later Life? Implications for Cognitive Health during Aging and the Treatment of Alzheimer’s Disease. Frontiers in Molecular Neuroscience 9, 53, July 2016.
- Folch et al.: The Involvement of Peripheral and Brain Insulin Resistance in Late Onset Alzheimer’s Dementia. Frontiers in Aging Neuroscience 11, 236, September 2019
- Fukuyama H et al: Altered Cerebral Energy Metabolism in Alzheimer’s Disease: A PET Study. Journal of Nuclear Medicine 35, no. 1 (1994): 1–6.
- den Heijer, T., et al. Homocysteine and brain atrophy on MRI of non-demented elderly. Brain 126 (Pt 1): 170–175 (2003).
- Gale SC et al: APOε 4 is associated with enhanced in vivo innate immune responses in humans. J Allergy Clin Immunol. 2014 Jul; 134(1): 127–134.e9.
- Henderson ST et al: Study of the ketogenic agent AC-1202 in mild to moderate Alzheimer's disease: a randomized, double-blind, placebo-controlled, multicenter trial. Nutrition & Metabolism volume 6, Article number: 31 (2009)
- Hernández F et al: GSK3: A possible link between beta amyloid peptide and tau protein. Experimental Neurology, Volume 223, Issue 2, June 2010, Pages 322-325.
- Hertz L et al: Effects of ketone bodies in Alzheimer's disease in relation to neural hypometabolism, β‐amyloid toxicity, and astrocyte function. Journal of Neurochemistry 134, no. 1, 7–20, July 2015.
- Loef M - Wallach H: The Omega-6/Omega-3 Ratio and Dementia or Cognitive Decline: A Systematic Review on Human Studies and Biological Evidence. J Nutr Gerontol Geriatr. 2013;32(1):1-23.
- Mirza A et al: Aluminium in brain tissue in familial Alzheimer’s disease. Journal of Trace Elements in Med Biol. Volume 40, March 2017, Pages 30-36.
- Montagne A et al: Alzheimer’s Disease: A Matter of Blood-Brain Barrier Dysfunction? Journal of Experimental Medicine 214, no. 11, 3151–69, November 2017
- de la Monte SM et al: Alzheimer’s Disease Is Type 3 Diabetes – Evidence Reviewed. Journal of Diabetes Science and Technology 2, no. 6, 1101–13, November 2008.
- Musiek ES et al: Sleep, Circadian Rhythms, and the Pathogenesis of Alzheimer Disease. Experimental & Molecular Medicine 47, no. 3 (2015)
- Mutter J et al: Does inorganic mercury play a role in Alzheimer's disease? A systematic review and an integrated molecular mechanism. J Alzheimers Dis. 2010;22(2):357-74.
- Kumar D et al: Amyloid-β peptide protects against microbial infection in mouse and worm models of Alzheimer’s diseas. Science Translational Medicine 25 May 2016.
- Kurakin A, Bredesen DE: Alzheimer’s disease as a systems network disorder: chronic stress/dyshomeostasis, innate immunity, and genetics. Aging 2020, Vol. 12, No. 18.
- Ott A et al: Diabetes Mellitus and the Risk of Dementia: The Rotterdam Study. Neurology 53, no. 9 (1999): 1937–42.
- Poole S et al: Determining the presence of periodontopathic virulence factors in short-term postmortem Alzheimer’s disease brain tissue. Journal of Alzheimer’s Disease 36: 665–677. (2013)
- Reiman EM et al: Functional brain abnormalities in young adults at genetic risk for late-onset Alzheimer's dementia. PNAS January 6, 2004 101 (1) 284-289.
- Talwar P et al: Systemic Immune Dyshomeostasis Model and Pathways in Alzheimer's Disease. Front Aging Neurosci . 2019 Oct 23;11:290.
- Tarasoff-Conway JM et al: Clearance Systems in the Brain—Implications for Alzheimer Disease. Nature Reviews. Neurology 11, no. (8) (2015): 457–70
- Safiah M et al: ApoE4: an emerging therapeutic target for Alzheimer's disease. BMC Med. 2019 Mar 20;17(1):64. doi: 10.1186/s12916-019-1299-4.
- Shi Y - Holtzman DM: Interplay between innate immunity and Alzheimer’s disease: APOE and TREM2 in the spotlight. Nat Rev Immunol. 2018 Dec; 18(12): 759–772.
- Qiu WQ et al: Insulin-Degrading Enzyme Regulates Extracellular Levels of Amyloid β-Protein by Degradation. Journal of Biological Chemistry 273, no. 49 (1998): 32730–8.
- Vasefi M et al: Diet Associated with Inflammation and Alzheimer’s Disease. J Alzheimers Dis Rep. 2019; 3(1): 299–309.
- Zhao N et al: Apolipoprotein E4 impairs neuronal insulin signaling by trapping insulin receptor in the endosomes. PMID: 28957663
