1. Colitis ulcerosa, fekélyes vastagbélgyulladás.
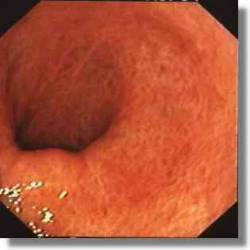 A colitis a vastagbél krónikus gyulladásos betegsége. Rendszerint alulról, a végbél környékéről indul ki, illetve ez a szakasz a legsúlyosabban érintett (proctitis). Súlyosabb esetben a vastagbél felsőbb szakaszai is betegek: a szigmabél, bal oldali vastagbél is gyulladásos. Legkiterjedtebb formájában a bélgyulladás a teljes vastagbélrendszert érintheti.
A colitis a vastagbél krónikus gyulladásos betegsége. Rendszerint alulról, a végbél környékéről indul ki, illetve ez a szakasz a legsúlyosabban érintett (proctitis). Súlyosabb esetben a vastagbél felsőbb szakaszai is betegek: a szigmabél, bal oldali vastagbél is gyulladásos. Legkiterjedtebb formájában a bélgyulladás a teljes vastagbélrendszert érintheti.
A colitis általában fiatal felnőttkorban jelentkezik. Első és legfőbb tünete az ismétlődő hasmenés. A hasmenéses széklet rendszerint véres, nyálkás jellegű. A laza széklet gyakran napi 10-15 alkalommal is jelentkezhet, az inger éjszaka is felébresztheti a beteget. Gyakran kíséri hasi fájdalom, különösen a bal alhas területén. Hőemelkedés, láz is társulhat a tünetekhez, és idővel vashiányhoz és vérszegénységhez vezethet.
A kivizsgálás során széklettenyésztéssel kell kizárni a hasmenés fertőzéses eredetet. A 3-4 hétnél tovább kitartó, tisztázatlan eredetű hasmenés esetén vastagbéltükrözést indokolt végezni. Ez tisztázhatja a gyulladásos bélbetegség tényét, súlyosságát, és kiterjedését. Szövettani mintavételnek kell történnie, mely a kórisme mikroszkopikus jellegzetességeit is igazolja.
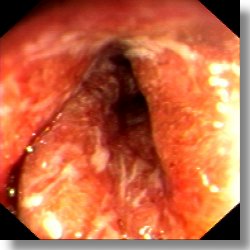 Az endoszkópia során enyhe fokú colitis esetén (felső kép) a nyálkahártya normális érrajzolatának eltűnik, a felszín finoman érdes. A kolonoszkóp fénye sokszorosan megtörve tükröződik vissza. A súlyos, aktív colitis (alsó kép) esetén az erősen vizenyős, vérbő és sérülékeny, törékeny nyálkahártyát összefolyó, elszórt fekélyek tarkítják. A fekélyeket fehér lepedék (fibrin) borítja. A fekélyes colitis elsősorban a vastagbél betegsége, de az autoimmun gyulladás más szerveken is jelentkezhet. Gyakran érintettek az ízületek, szemek és bőr. A bélen kívüli megjelenési formák esetenként évekig elterelhetik a figyelmet a bélbetegségről.
Az endoszkópia során enyhe fokú colitis esetén (felső kép) a nyálkahártya normális érrajzolatának eltűnik, a felszín finoman érdes. A kolonoszkóp fénye sokszorosan megtörve tükröződik vissza. A súlyos, aktív colitis (alsó kép) esetén az erősen vizenyős, vérbő és sérülékeny, törékeny nyálkahártyát összefolyó, elszórt fekélyek tarkítják. A fekélyeket fehér lepedék (fibrin) borítja. A fekélyes colitis elsősorban a vastagbél betegsége, de az autoimmun gyulladás más szerveken is jelentkezhet. Gyakran érintettek az ízületek, szemek és bőr. A bélen kívüli megjelenési formák esetenként évekig elterelhetik a figyelmet a bélbetegségről.
A colitis általában mérsékelt aktivitást és hullámzó lefolyást mutat, de alkalmankánt olyan súlyos, egész vastagbelet érintő agresszív gyulladás képével jelentkezik (toxikus megacolon), hogy csak a teljes vastagbélrendszer sürgős eltávolításával lehet megmenteni a beteg életét.
2. Crohn-betegség, ileitis terminalis
A krónikus gyulladásos bélbetegségek másik típusa régebben jellemzően fiatal felnőttkorban jelentkezett, de manapság egyre gyakrabban találjuk idősödő betegekben is. A teljes tápcsatornát bárhol érintheti, bizonyos szakaszokat érintetlenül hagyva, másokat foltokban megbetegítve. A "klasszikus" Crohn-betegség a vékonybél utolsó szakaszát, a vékonybél-vakbél átmenetének területét érinti a jobb alhasban (terminális ileum). Míg a colitis elsősorban a bél nyálkahártyát betegíti, addig itt a teljes falát érinti a gyulladás, ezért a bélfal megvastagodik, tömötté válik. Esetenként inkább heges szűkületeket okoz a gyulladás, máskor a bélfal átfúródik, és sipolyok keletkeznek egyes bélszakaszok között. A hasfalra vagy gáttájékra kitört járat sem ritka.
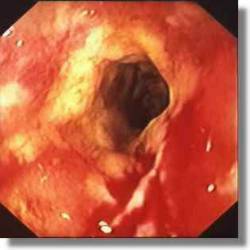 A Crohn-betegség tünetei meglehetősen változatosak. A típusos vékonybél-vastagbél lokalizáció esetén visszatérő jobb alhasi jellegű görcsös fájdalmak jelentkeznek, ezért nem ritkán "vakbélgyulladás" gyanújával végzett műtét során derül ki a betegség. Máskor számos vizsgálat történik, mielőtt a betegséget igazolni sikerül. A hosszas betegség rendszerint a laboreredményekben is kóros gyulladásos képet, vashiányos vérszegénységet eredményez. Hasznos, nem invazív lehetőség a széklet calprotectin vizsgálat, mely érzékenyen mutatja a bélrendszerben zajló gyulladást, és az irritábilis bél szindrómától is jól elkülöníti a panaszokat.
A Crohn-betegség tünetei meglehetősen változatosak. A típusos vékonybél-vastagbél lokalizáció esetén visszatérő jobb alhasi jellegű görcsös fájdalmak jelentkeznek, ezért nem ritkán "vakbélgyulladás" gyanújával végzett műtét során derül ki a betegség. Máskor számos vizsgálat történik, mielőtt a betegséget igazolni sikerül. A hosszas betegség rendszerint a laboreredményekben is kóros gyulladásos képet, vashiányos vérszegénységet eredményez. Hasznos, nem invazív lehetőség a széklet calprotectin vizsgálat, mely érzékenyen mutatja a bélrendszerben zajló gyulladást, és az irritábilis bél szindrómától is jól elkülöníti a panaszokat.
A Crohn-betegség kórismézése rendszerint nehéz feladat, de a gyanú felvetése már fél győzelem lehet. Ilyenkor a vastagbéltükrözés során az utolsó vékonybélszakaszig kell felvezetni az endoszkópot. Mivel a kórkép szájtól a végbélnyílásig a teljes tápcsatornán előfordulhat, ezért a gyomortükrözést, és a vékonybelek speciális radiológiai vizsgálatait is el kell végezni.
A megfelelően kezelt Crohn-betegség sokszor éveken keresztül tünetmentesen visszaszorítható (remisszió), máskor szinte megállíthatatlanul sodródik a beteg egyik szövődményből a másikba. A kezelési taktikában a végsőkig kitartunk a gyógyszeres kezelés mellett, és csak komoly bélszűkületek, vagy sipolyok esetén végezzük el a legszükségesebb sebészi beavatkozásokat.
Mi okozza?
Mai tudásunk szerint az IBD-nek nincs egyetlen konkrét oka. A hajlamosító genetika, a mérgesebb bélflóra, ill. bélfalat károsító környezet együttesen formálja a betegséget.
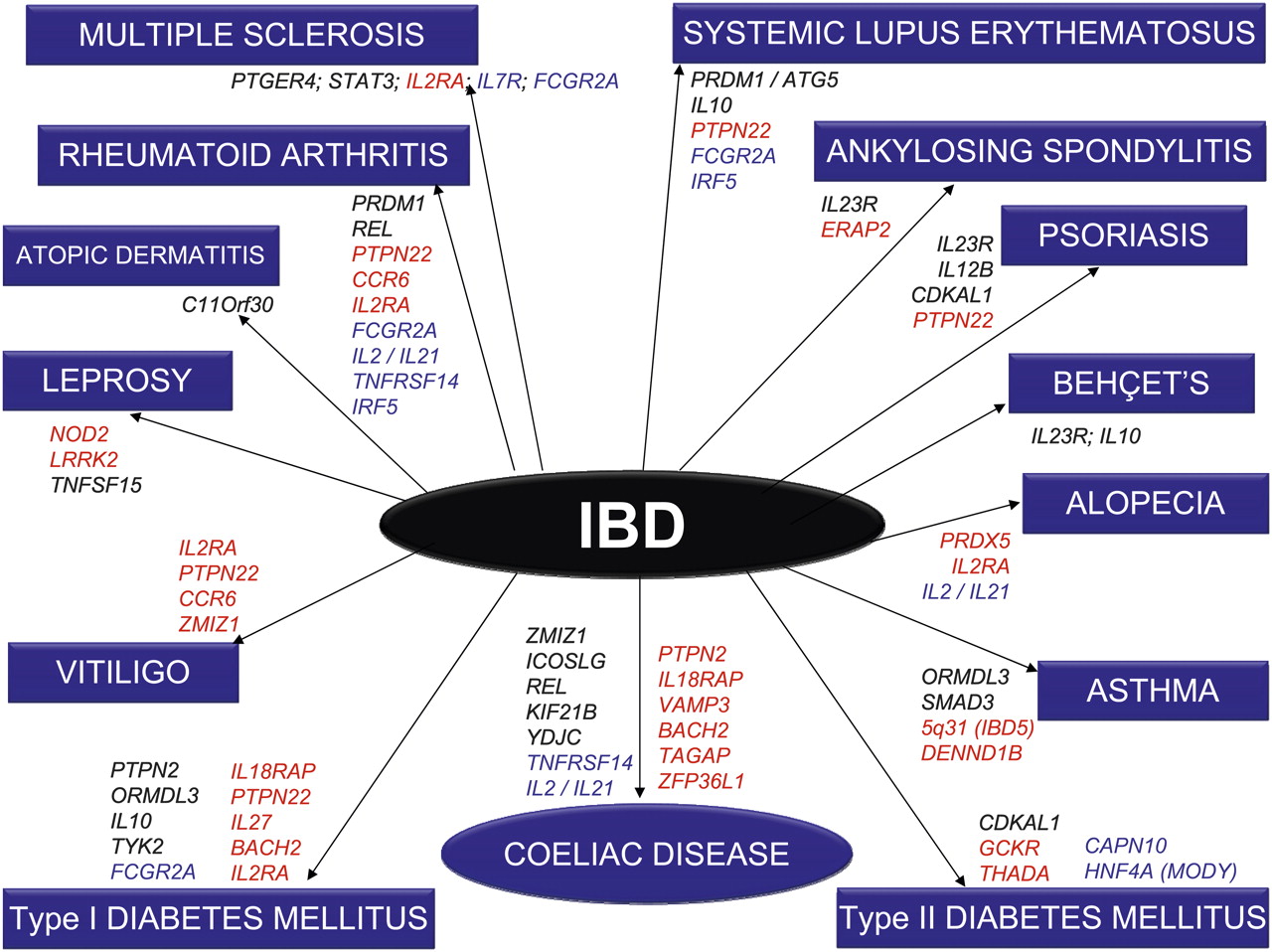
Nincs olyan kitüntetett génhiba, mely egyértelműen IBD-t okozna, ugyanakkor legalább 99 olyan gént ismerünk, amelyik többé-kevésbé hajlamosít a krónikus bélgyulladásra. Ugyanezen génváltozatok számos további gyulladásos-autoimmun betegségre is fogékonnyá tesznek (ábra).®
A genetikai hozományon túl is meghatározó a környezet szerepe, hiszen az emúlt évtizedekben durván szaporodik mindkét típusú IBD (és a többi gyulladásos-autoimmun betegség).® Amint az iparosodás és "jólét" útjára tér egy ország: látványosan terjedni kezd az IBD.® Az urbanizált környezethez erősen feldolgozott, adalékolt és tartósított étrend tartozik, amit antibiotikumok és antiszeptikumok kiterjedt használata kísér.® A civilizációs ártalom jelentősen elszegényíti, átformálja a normálisnak tartható emberi bélflórát, és megzavarja a lakóközösség valamint gazda békés viszonyát.
Az egészséges bélfal, és a benne lakó milliárdnyi paránylény között egy ingatag frontvonal húzódik. Az immunrendszer kiegyezik az aktuális bélflórával egy távolságban, mely még elfogadható a zavartalan együttéléshez. A bél falát egyetlen sejtvonal (drótkerítés) védi, mely előtt egy demilitarizált övezet (nyákréteg) fekszik, ami akadályozza a baktériumok mozgását. Határőrök dolgoznak az illegális behatolók kiszűrésén. A kerítés mentén határvadászok (un. Paneth sejtek) lőnek mindenre, ami megközelíti a határvonalat. Persze, mindig van, aki bejut a frontvonal mögé. A beszivárgó titkos ügynököket lekapcsolni a belső elhárítás dolga.® A mélységi akciók után a lakossági pánikot lecsendesítik, majd a frontvonalak mögött visszaáll a törékeny béke. Az immunrendszerben számos beépített fék van, melyek dolga a "veszélytelen" jelzésekre adott gyulladásos válasz megállítása. Ha valahol megbomlik a törékeny egyensúly, akkor tartós polgárháború alakul, melyben mindenki sérül.
Crohn-betegségben egyaránt szerepet játszhat a gyengült határ-védelem (NOD2 mutáció, Paneth-sejt diszfunkció), vagy a rossz hatékonyságú belső elhárítás (autofágia zavara).® Ellenállás hiányában a mikróbák belakják a határvidéket (nyákréteg), és egyre többen átjutnak a kerítésen. Ez jellegzetesen vékonybélre lokalizált, és fiatal korban megjelenő betegséget okoz.® Máskor éppen a bélfal immunsejtjeinek túlzott ingerlékenysége okoz felesleges pánikot (Th1, Th17 immunválasz).® Az elszabadult gyulladás a bélfal mélyebb rétegeiben zajlik, ezért hegesedés, átfúródás, tályog, sipolyok alakulása lehet a következmény.
Colitis esetén kisebb jelentősége van a genetikai tényezőnek, és erősebben felmerül az agresszívabb bélflóra szerepe,® és a határvidék károsodása (áteresztő bélfal).® A patogén flóra belakja a gyengült nyákréteget, a tolerálhatónál közelebb húzódó betolakodók pedig védekező választ provokálnak. Colitisben az ütközőzóna felszínesebb, ezért főként a nyálkahártya-réteg károsodik.®
A bélfalon alakuló viszonylag stabil frontvonal tehát egy kölcsönös kiegyezés (immuntolerancia) eredménye a mikrobiom és gazda között. A bélgyulladás formálásában (személyre szabottan, különböző mértékben) mindig három tényező játszik szerepet: a "támadó" bélflóra, a károsodott bélfal, és a paranoid védekező válasz.
Az IBD terápiája.
⇒ Gyulladás-csökkentő terápia. A gyulladásos bélbetegségek klasszikos orvosi kezelése a gyulladás megfékezésére fókuszál. Hagyományos gyógyszereink (Salazopyrin, Salofalk, Imuran, szteroidok) mindegyike potens gyulladáscsökkentő. A "biológiai" kezelés (pl.: Humira) ígéretesen szép neve ellenére ugyanezt teszi: célirányosan kiüti a gyulladásos folyamat egyes kulcsfontosságú elemeit. Sajnos nem csak a bélben. A gyulladáscsökkentő kezelés hatékonyan lehűti a paranoid immunrendszert, ugyanakkor számos mellékhatás kíséri. Ráadásul, mint láttuk: a gyulladás-hajlam csak egyik tényező a három közül.
⇒ A bélflóra átalakítása.
A fogantatástól felnőttkorig mindenkiben alakul egy személyre szabott, viszonylag stabil mikrobiom (un. entero-típus).® A betegekben található lakóközösség néha látványosan (máskor kevésbé) különbözik az egészséges bélflórától, és jellegzetesen csökken annak diverzitása.® Annyi bizonyos, hogy a beteg nem képes békességben élni a benne lakó elszegényedett közösséggel, és úgy fest, hogy éppen ettől beteg. Erre utal, hogy sok betegben tudunk olyat bélflórát alakítani, amivel jobban kijön.
A probiotikumok néhányféle (max. egy tucatnyi) jótékony mikrobát tartalmaznak, melyek "felülírják" a bélflórát. Ez persze nem lesz tartós, és nem pótolhatja az egészséges közösség változatosságát, de a patogének kiszorításával colitis ulcerosa esetén mégiscsak segíthet valamit. Crohn-betegségben alig.®
A féregnyúlvány ("vakbél") eltávolítása a makacs colitis esetén meglepően gyakran (az esetek harmadában) javulást hoz.® Ez a csökevényes zsákutca ugyanis rezervoár-ként raktározza a megszokott (és adott esetben betegítő) bélflórát. A vakbélműtét után a mikrobiom "memóriája" elvész, így könnyebben épülhet új flóra. Az ép "vakbél" eltávolítása ma még ritkán merül fel, de másra nem reagáló colitis esetén a jövőben elterjedhet.
A széklet-transzplantáció (Fecal Microbiota Transplantation, FMT) ígéretes módszerünk az ép, egészséges bélflóra "beültetésére". Az FMT látványosan gyógyítja a Clostridium által okozott bélgyulladást,® és IBD esetén is számos sikeres próbálkozásról van tudomásunk.® Azonban számos kérdés ma sem tisztázott. Nem tudjuk a donorszéklet optimális kezelési módját, nem tudjuk hogyan legjobb bejuttatni, adjunk-e antibiotikumot előtte, hányszor érdemes ismételni, és meddig tart a hatása. Végül a legnagyobb probléma: ma sem tudjuk, hogy ki az optimális donor, és a nyugati országokban egyre nehezebb egészséges, gazdag flórával élőt találni. A kétségek ellenére az FMT már felbukkant a terápiás ajánlások között, de még sok kutatást igényel a minőségi standardok kidolgozása.
⇒ Áteresztő bélfal regenerálása.
A "lyukas kerítés" egyértelműen hozzájárul a bélfalban alakuló polgárháborúhoz. Egy friss vizsgálatban az áteresztő bélfal háromszorosára emelte a Crohn-betegség kialakulásának kockázatát.® A "lyukas" bélfal évekkel megelőzte a bélgyulladást, tehát nem következménye, hanem forrása volt a gyulladásnak! De mi okozhat áteresztő bélfalat?®
- Napi cirkadián ritmus felborulása, alváshiány.
- Pszichés stressz, és extrém fizikai terhelés.
- Alkohol, és számos gyógyszer (aszpirin, nem szteroid gyulladásgátlók, kemoterápia).
- Élelmiszeripari emulgeátorok (karragén, poliszorbát, karboximetilcellulóz, stb.)
- Cukoralkoholok, mesterséges édesítők (szorbit, mannit, xilit)
- Növényi lektinek, és kiemelten a gabona-glutén.
- Bizonyos baktérium-típusok (diszbakteriózis).
Fontos kiemelni, hogy a genetikai gyulladás-hajlamunk születéstől adott, de a fentiek lehetőséget kínálnak a változtatásra. A bélfal regenerálására önmagában persze kevés lehet gyógyuláshoz, de miután kórosan áteresztő bél a betegség egyik lehetséges oka, így minden egyes betegnél törekedni kell annak felszámolására!
IBD és diéta.
Nem kérdéses, hogy a gyulladásos bélbetegség összefügg a gagyi nyugati diétával.® és a bélflóra látványosan igazodik az étrendhez.® De hogy mit kellene helyette enni? Nos, arról lényegében fogalmunk sincs.® Ennek tudható, hogy a gyakorló bélbetegek évek során a létező összes étrendi jótanácsot végigpróbálják, mielőtt feladják a reményt. A következőt azoknak ajánlom, akik még nem adták fel.
A húsevő (ragadozó, carnivore) étrendi ajánlás arra alapoz, hogy a bélfal sérülését provokáló növényi források kiiktatása meglepő javulást eredményezhet.® A gabonafélék, növényi lektinek (hüvelyesek, paradicsom, paprika, padlizsán, stb), finomított cukorfélék, cukoralkoholok, növényi olajok, olajos magvak elhagyása szinte minden betegnek előnyére válhat. Egyéni érzékenységtől függően mellőzendő a tej, tejtermékek (esetenként a tojás-fehérje is). Helyettük az étrend a nutriensekben bővelkedő, könnyen emészthető minőségi húsfélékre alapoz. Legjobb a szabadon tartott kecske, birka, marha, bivaly, és vadhús ill. halféle, de a tanyasi kapirgálós jérce, gyöngytyúk, kacsa is minden pénzt megér. Az antibiotikumtól mentes, minőségi forrás itt kulcsfontosságú lehet. Különösen megbecsülendők az említett jószágokból származó zsiradékok, belsőségek, és jól elkészített inas-csontos-porcos húslé. A tojás sárgájának lipidjei, és különösen a lecitin: pedig a colitis speciális gyógyszere! ®
Ez a csapásirány határozottan szembemegy az általános diétás ajánlásokkal, de szerintem ez senkit sem izgat, ha történetesen éppen ettől marad remisszióban a betegsége. Angolul értőknek íme egy kis motíváció.
- Arumugam M et al: Enterotypes of the human gut microbiome. Nature. 2011 May 12; 473(7346): 174–180.
- Brand S: Crohn's disease: Th1, Th17 or both? The change of a paradigm: new immunological and genetic insights implicate Th17 cells in the pathogenesis of Crohn's disease. Gut. 2009 Aug;58(8):1152-67.
- Boussard JL, Devkota S: The changing microbial landscape of Western society: Diet, dwellings and discordance. Mol Metab. 2016 Sep; 5(9): 737–742.
- Burisch J, Munkholm P: The epidemiology of inflammatory bowel disease. Scand J Gastroenterol. 2015 Aug;50(8):942-51.
- Camilleri M: Leaky gut: mechanisms, measurement and clinical implications in humans. Gut. 2019 Aug;68(8):1516-1526.
- David LA et al: Diet rapidly and reproducibly alters the human gut microbiome. Nature. 2014 Jan 23;505(7484):559-63.
- Johansson MEV et al. Bacteria penetrate the normally impenetrable inner colon mucus layer in both murine colitis models and patients with ulcerative colitis. Gut. 2014;63 (2):281–291.
- Kaplan GG, Windsor JW: The four epidemiological stages in the global evolution of inflammatory bowel disease. Nature Reviews Gastro & Hep vol 18, pages56–66(2021)
- Keshteli AH et al: Diet in the Pathogenesis and Management of Ulcerative Colitis; A Review of Randomized Controlled Dietary Interventions. Nutrients. 2019 Jul; 11(7): 1498.
- Khalili H et al. The role of diet in the etiopathogenesis of inflammatory bowel disease. Nat Rev Gastroenterol Hepatol. 2018 Sep; 15(9): 525–535.
- Khan I et al: Alteration of Gut Microbiota in Inflammatory Bowel Disease (IBD): Cause or Consequence? IBD Treatment Targeting the Gut Microbiome. Pathogens. 2019 Sep; 8(3): 126.
- Lees CW et al: New IBD genetics: common pathways with other diseases. Gut. 2011 Dec;60(12):1739-53.
- Li YT et al: Systematic review with meta-analysis: long-term outcomes of faecal microbiota transplantation for Clostridium difficile infection. Aliment Pharmacol Ther. 2016 Feb;43(4):445-57.
- Lopez J, Grinspan A: Fecal Microbiota Transplantation for Inflammatory Bowel Disease. Gastroenterol Hepatol (N Y). 2016 Jun; 12(6): 374–379.
- Michielan A, D'Inca R: Intestinal Permeability in Inflammatory Bowel Disease: Pathogenesis, Clinical Evaluation, and Therapy of Leaky Gut. Mediators Inflamm. 2015; 2015: 628157.
- Sahami S et al: Appendectomy for Therapy-Refractory Ulcerative Colitis Results in Pathological Improvement of Colonic Inflammation: Short-Term Results of the PASSION Study. J Crohns Colitis. 2019 Feb 1;13(2):165-171.
- Sidiq T et al: Nod2: A Critical Regulator of Ileal Microbiota and Crohn’s Disease. Front Immunol. 2016; 7: 367.
- Shen Z-H et al: Relationship between intestinal microbiota and ulcerative colitis: Mechanisms and clinical application of probiotics and fecal microbiota transplantation.
- Silva NO et al: Probiotics in inflammatory bowel disease: Does it work? World J Meta-Anal. Apr 28, 2020; 8(2): 54-66 J Gastroenterol. 2018 Jan 7; 24(1): 5–14.
- Stange EF, Schroeder BO: Microbiota and mucosal defense in IBD: an update. Expert Rev Gastroenterol Hepatol. 2019 Oct;13(10):963-976.
- Stremmel W et al: Delayed release phosphatidylcholine as new therapeutic drug for ulcerative colitis--a review of three clinical trials. Expert Opin Investig Drugs. 2010 Dec;19(12):1623-30.
- Tóth C, Dabóczi A, Howard M, Miller NJ, Clemens Z. Crohn's disease successfully treated with the paleolithic ketogenic diet. Int J Case Rep Images 2016;7(10):570–578.
- Turpin W...Croitoru K: Increased Intestinal Permeability Is Associated With Later Development of Crohn's Disease. Gastroenterology. 2020 Dec;159(6):2092-2100.e5.
- Wehkamp J, Stange EF: An Update Review on the Paneth Cell as Key to Ileal Crohn's Disease. Front Immunol. 2020 Apr 15;11:646.